Un recién nacido con una enfermedad metabólica letal recibió la primera terapia CRISPR personalizada del mundo, diseñada solo para él. Los resultados iniciales muestran que su organismo empezó a funcionar como si la mutación nunca hubiera existido.
Por Alina C. Galifante para NLI
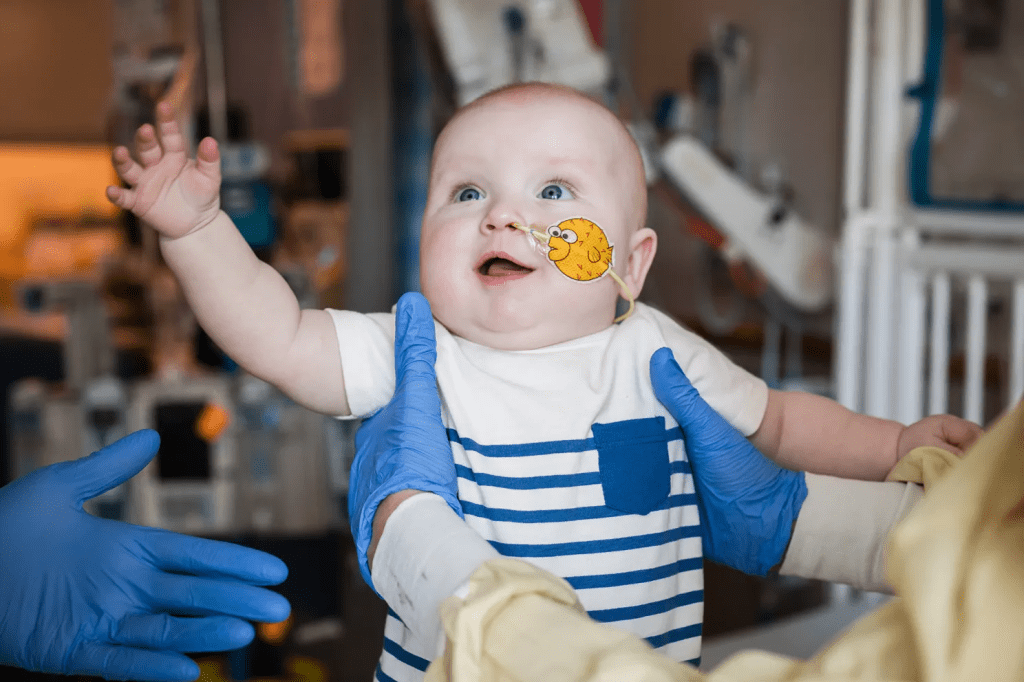
Un caso que cambia la historia de la medicina
El protagonista es un bebé con una mutación gravísima en el gen CPS1, responsable de un trastorno metabólico que impide procesar adecuadamente el amoníaco. Sin tratamiento, la acumulación tóxica puede provocar daño cerebral irreversible o la muerte en cuestión de horas. Hasta ahora, las opciones eran dietas extremas, medicación constante y, con suerte, trasplante hepático. Nada que se acerque a una cura.
En este niño, cuentan desde Nature, los médicos hicieron algo distinto: construyeron una terapia genética desde cero, pensada únicamente para la variante exacta de su ADN.
Y lo hicieron en un tiempo récord: seis meses entre diagnóstico, diseño y aplicación.
Cómo se reparó un gen en pleno funcionamiento
La intervención utilizó CRISPR base editing, una herramienta capaz de corregir una sola “letra” del ADN sin cortar la doble cadena. Esta precisión quirúrgica reduce riesgos y permite reescribir la mutación sin alterar otras zonas del genoma.
El editor genético viajó en nanopartículas lipídicas, similares a las usadas en las vacunas de ARN, y fue dirigido específicamente al hígado, la fábrica metabólica del organismo. Allí comenzó a actuar sobre las células enfermas.
A los pocos meses, el cambio fue evidente: el bebé toleró más proteínas, dejó de depender de medicación constante para evitar crisis tóxicas y, frente a una infección respiratoria —situación que normalmente desencadena catástrofes metabólicas—, no presentó complicaciones graves. Para los especialistas, eso es una señal inusual de recuperación funcional real.
Lo que promete y lo que todavía falta
Aunque los resultados son impresionantes, esta técnica no es una solución universal. Cada tratamiento debe diseñarse a medida, mutación por mutación, paciente por paciente. Implica costos elevados, una carrera contra el tiempo y enormes desafíos regulatorios.
Además, todavía no se sabe si la edición será estable a largo plazo, si requerirá refuerzos o si pueden aparecer efectos adversos con los años. Es un primer paso gigantesco, sí, pero todavía un paso.
De todos modos, el caso del “Paciente Eta” ya reconfiguró el tablero. Por primera vez, la medicina mostró que puede fabricar terapias que encajen en un genoma como llave en cerradura, acelerando el camino hacia una “CRISPR para uno”.
Y si este experimento continúa funcionando, la pregunta deja de ser si la medicina personalizada extrema es posible y pasa a ser cuándo estará disponible para los demás.
Descubre más desde Noticias La Insuperable
Suscríbete y recibe las últimas entradas en tu correo electrónico.

